凱氏定氮法是由丹麥化學家凱道爾于1883年建立的,現已發展為常量、微量、平微量凱氏定氮法以及自動定氮儀法等,是分析有機化合物含氮量的常用方法。 凱氏定氮法的理論基礎是蛋白質中的含氮量通常占其總質量的16%左右(12%~一19%),因此,通過測定物質中的含氮量便可估算出物質中的總蛋白質含量(假設測定物質中的氮全來自蛋白質),即: 蛋白質含量=含氮量/16%。
凱氏定氮法是測定化合物或混合物中總氮量的一種方法。即在有催化劑的條件下,用濃硫酸消化樣品將有機氮都轉變成無機銨鹽,然后在堿性條件下將銨鹽轉化為氨,隨水蒸氣蒸餾出來并為過量的硼酸液吸收,再以標準鹽酸滴定,就可計算出樣品中的氮量。由于蛋白質含氮量比較恒定,可由其氮量計算蛋白質含量,故此法是經典的蛋白質定量方法。
凱式常量定氮儀
以GB/T 12309-1990 工業玉米淀粉為例講解實驗過程
a.分解:稱取混勻的樣品3~4g(精確至0.001g),放入干燥的凱氏燒瓶中(避免樣品粘在瓶頸內壁上),加入復合催化劑10g、硫酸25mL和幾粒玻璃珠,輕輕搖動燒瓶,使樣品完全濕潤。然后將凱氏燒瓶以45度角斜放于支架上,瓶口蓋以玻璃漏斗,用電爐開始緩慢加熱,當泡沫消失后,強熱至沸。待瓶壁不附有炭化物時,且瓶內液體為澄清淺綠色后,繼續加熱30min,使其完全分解(以上操作應在通風櫥內進行)。

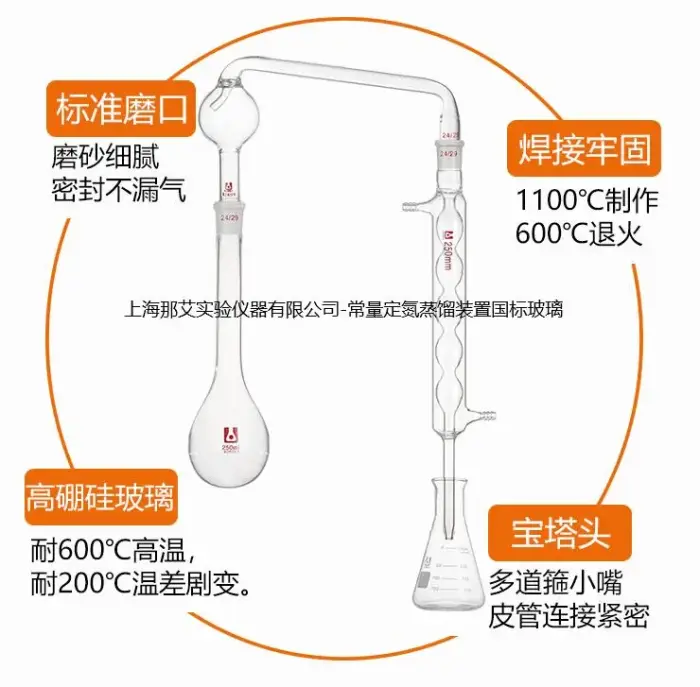
常量定氮蒸餾裝置
b.蒸餾:待分解液冷卻后,用蒸餾水沖洗玻璃滯斗及燒瓶瓶頸,并稀釋至200mL,將凱氏燒瓶移于蒸餾架上,在冷凝管下端接500mL錐形瓶作接收器,瓶內預先注入2%硼酸溶液50.0mL及混合指示液10滴。將冷凝管的下口插入錐形瓶的液體中,然后沿凱氏燒瓶頸壁緩慢加入40%氫氧化鈉溶液70~100mL,打開冷卻水.立即連接蒸餾裝置,輕輕搖動凱氏燒瓶,使溶液混合均勻,加熱蒸餾,至餾出液為原體積的3/5時停止加熱。使冷凝管下口離開錐形瓶,用少量水沖洗冷凝管,洗液并入錐形瓶中。
c.滴定:將錐形瓶內的液體用0.05mol/L硫酸標準溶液滴定,使溶液由藍綠色變為灰紫色,即為終點。

